1. LES ACIERS
La norme ISO 898-1:2013 spécifie les caractéristiques mécaniques et physiques des vis, tiges filetées et autres éléments constituant les chevilles en acier au carbone et en acier allié, testé dans la plage de température ambiante de 10°C à 35°C.
Les aciers standards les plus couramment utilisés pour la fabrication de chevilles sont répertoriés selon leur classe de résistance, comme indiqué dans le tableau ci-après : dans lequel fuk indique la tension de rupture caractéristique et fyk la limite élastique caractéristique de l’acier.
There is no table associated with this shortcode.
Les aciers sont généralement protégés contre la corrosion par un revêtement additionnel. Les principaux types de traitement sont le zingage ou la galvanisation à chaud.
Le zingage consiste à surcoucher l’acier d’un revêtement de zinc de 5 μm, selon la norme EN ISO 4042.
La galvanisation à chaud, ou plus exactement la « galvanisation à chaud au trempé», est une technique de l’industrie de lamétallurgie qui est utilisée pour renforcer une pièce d’acier à l’aide de zinc, dans un bain de zinc en fusion à 450°C environ.
Ce procédé donne au revêtement protecteur de l’adhérence, de l’imperméabilité, et de la résistance mécanique. Une pièce traitée par la galvanisation est dite galvanisée.
C’est un principe qui conjugue les 2 types de protection, physique par enrobage de la pièce, et chimique par apport d’un métal. Le traitement doit être conforme à la norme ISO 1461 («Revêtements par galvanisation à chaud sur produits finis en fonte et en acier »). Ce procédé ne consiste pas uniquement à déposer du zinc sur quelques micromètres à la surface de l’acier.
Le revêtement de zinc est chimiquement lié à l’acier de base, car il se produit une réaction chimique métallurgique de diffusion entre le zinc et le fer ou l’acier. Quand on retire l’acier du bain, il s’est formé à sa surface plusieurs couches d’alliages zinc-fer sur lesquelles le zinc entraîné se solidifie.
Ces différentes couches d’alliages plus dures que l’acier de base pour certaines, ont une teneur en zinc de plus en plus élevée au fur et à mesure que l’on se rapproche de la surface du revêtement.
LA GALVANISATION
AVANTAGES
- La galvanisation permet d’obtenir un enrobage total de la pièce (intérieur et extérieur), sans qu’aucune zone ne soit laissée sans protection, c’est donc de très loin la protection la plus efficace.
- La galvanisation a l’avantage de la « double protection » :
- Protection physique par enrobage,
- Protection électrochimique (le pouvoir sacrificiel du zinc).
- L’épaisseur du revêtement est importante : 45 microns.
- le revêtement après galvanisation est très adhérent : il se crée un alliage métallique.
INCONVÉNIENTS
- La galvanisation consistant à plonger les pièces dans un bain de zinc en fusion à 450°C, il en résulte des risques de déformation des pièces fines.
- Résidus de zinc lors de la sortie de la pièce, (coulures, grattons, etc.) et irrégularités de surface dues à l’épaisseur de zinc déposée 45 microns). Ces irrégularités d’aspect inhérentes au traitement ne peuvent pas être considérées comme des défauts.
- Les trous et filetages sont obstrués par le zinc en fusion, ce qui nécessite un perçage ultérieur.
- Difficulté à peindre car il y a des risques de dégazage lors du thermolaquage ultérieur avec apparition de bullage de surface.
Le zingage électrolytique occupe une position dominante dans le domaine de la galvanoplastie par le tonnage de métal électro-déposé. Les dépôts de zinc brillants sont très largement répandus et les électrolytes se sont développés pour donner aux dépôts des propriétés recherchées en termes d’aspect décoratif, de résistance à la corrosion et d’aptitude à la passivation au chrome. Le zingage électrolytique est appliqué pour résister d’abord à la corrosion avant toute considération esthétique ou fonctionnelle. La protection contre la corrosion de l’acier est d’abord le fait de la différence de potentiel anodique entre le zinc et le fer contenu dans l’acier. L’acier est ainsi protégé par protection cathodique aussi longtemps que le zinc ne sera pas complètement oxydé. La capacité du dépôt à réduire la vitesse de corrosion se résume simplement à 4 variables :
- L’épaisseur du dépôt communément située à 5 microns aujourd’hui ;
- Sa capacité à recevoir des couches de conversion protectrices d’épaisseurs de l’ordre de 200 à 400 nm dans le cas des conversions au chrome trivalent ;
- La diminution de la différence de potentiel avec l’acier par l’utilisation d’alliages plus nobles tels que le Zn-Ni à 12-15 % en nickel ;
- Le dépôt d’une finition renforcée de type organo-minérale utilisant de la silice, des lubrifiants et des inhibiteurs sur une épaisseur de 1 μm.
Les électrolytes de zingage se répartissent en 2 types : alcalins ou acides.
L’ÉLECTRO ZINGAGE
AVANTAGES
- Cette technique est plus douce que la galvanisation.
- L’électro-zinguage permet le traitement sans déformation.
- La surface obtenue est extrêmement lisse, et après peinture on obtient un aspect parfait.
- Le revêtement est très adhérent.
INCONVÉNIENTS
- Épaisseur du revêtement moins importante
Les aciers inoxydables, couramment appelés inox sont des aciers auxquels on ajoute une forte proportion de chrome (> à 10,5 %). Cet élément leur confère une excellente résistance à la corrosion, une inoxydabilité. Le but des aciers inoxydables est d’avoir un matériel en acier très résistant à la rouille et la corrosion et résistant aux :
- Conditions atmosphériques défavorables tel que le dioxyde de carbone, l’humidité, les champs électriques, le soufre, le sel, et les composés de chlorure.
- Substances chimiques produites naturellement ou artificiellement (par exemple : l’ozone).
- Conditions extrêmes telles que des températures très élevées.
L’acier inoxydable est 100 % recyclable. En fait, plus de 50 % d’un nouvel acier inoxydable est fait à partir des chutes de métal refondu, le rendant bon pour l’environnement. La norme DIN EN ISO 3506 s’applique aux vis et écrous en acier inoxydable. Il existe un grand nombre d’aciers inoxydables qui sont répartis en trois sous-groupes :
- Les aciers austénitiques (les plus courants).
- Les aciers ferritiques.
- Les aciers martensitiques.
Système d'identification ISO pour le groupe des aciers austénitiques :
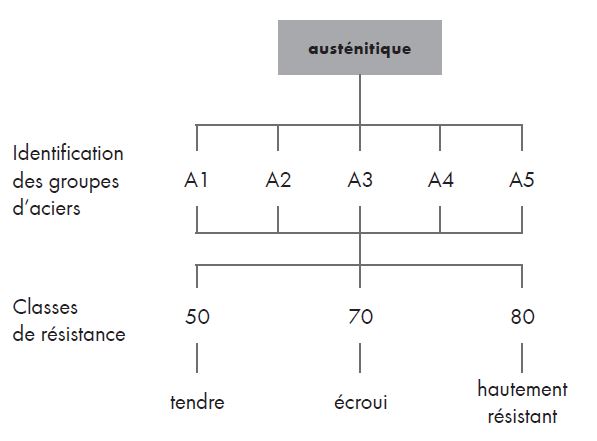
Il y a plus de 150 types d’acier inoxydable, classés en diff érentes catégories selon la composition.
Composition des aciers inoxydables les plus courants
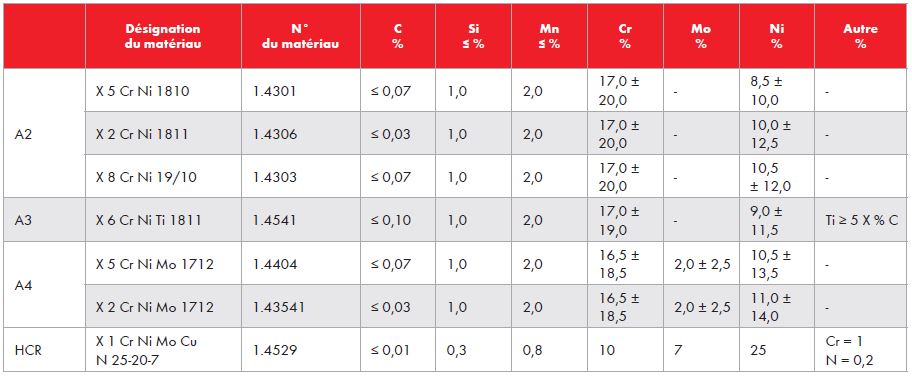
En cas de sollicitations corrosives importantes, il convient d’utiliser des aciers chrome – nickel – molybdène du groupe A4. Seules les chevilles en inox A4 peuvent être posées à l’extérieur conformément à leur ATE. Si l’on s’appuie sur l’Eurocode 3 « Calcul de structures en acier » NF EN 1993-1-4, on peut lire en annexe A 4.1 que la nuance d’inox dite HCR (Haute Résistance à la Corrosion) [1.4529] est adaptée aux applications structurelles en environnement marin à risque élevé et tunnel routier avec salage. Comme par exemple les fixations d’éléments porteurs situés dans des atmosphères chargées en chlorures ne pouvant faire l’objet d’un nettoyage régulier avec une eau contenant plus de 250 mg/l d’ions chlorures. (voir tableau ci-contre) La norme allemande Z30.3-6 va encore plus loin en le préconisant pour les stations thermales (présence d’ion chlorure et de chaleur).
3. PHÉNOMÈNES DE CORROSION DE L’ACIER
La corrosion désigne l’altération d’un objet manufacturé par l’environnement. La corrosion a des causes à la fois physico-chimiques et mécaniques.
Les exemples les plus connus sont les altérations chimiques des métaux dans l’eau (avec ou sans oxygène), tels la rouille du fer et de l’acier ou la formation de vert-de-gris sur le cuivre et ses alliages (bronze, laiton). Dès qu’un métal est en présence d’oxygène, son oxydation commence instantanément. La corrosion des métaux est un phénomène naturel.
La corrosion des métaux est dans la grande majorité des cas une réaction électrochimique (une oxydoréduction) qui fait intervenir la pièce manufacturée et l’environnement.
Le matériau dont est faite la fixation n’est pas le seul facteur conditionnant la vitesse du processus d’oxydation, puisque la forme de la pièce et les traitements subis (mise en forme, soudure, vissage) jouent un rôle primordial. On distingue la corrosion généralisée qui se forme lorsque l’acier inoxydable est en contact avec un milieu acide et la corrosion localisée qui se rencontre dans la majorité des cas lorsque l’inox est placé dans un milieu neutre chloruré. Le processus de corrosion peut également être ralenti en agissant sur la réaction chimique en elle-même.
Il existe 3 types de corrosion :
- La corrosion par contact.
- La corrosion par piqûres.
- La corrosion sous contraintes.
La corrosion par contact naît d’un assemblage de 2 métaux différents (par exemple 2 nuances d’aciers, ou le même acier traité différemment), peut créer une corrosion accélérée ; on voit d’ailleurs souvent des traces de rouille au niveau des écrous. La corrosion est donc un phénomène qui dépend du matériau utilisé, de la conception de la pièce (forme, traitement, assemblage) et de l’environnement.
There is no table associated with this shortcode.
Très recommandé : +++
Assez recommandé : ++
Recommandé : +
Peu recommandé : —
Pas recommandé : —
Pas du tout recommandé : –
La corrosion par piqûre est la rupture locale du film de passivation de l’acier inoxydable provoquée par un électrolyte riche en chlorures et/ou sulfures. A l’endroit de la piqûre, le métal est mis à nu, la corrosion va se développer si la piqûre ne se repassive pas, donc si la vitesse de dissolution du métal permet de maintenir un environnement suffisamment agressif pour empêcher sa repassivation. On désigne par « corrosion sous contrainte » la formation de fissures qui démarrent après une période d’incubation plus ou moins longue et qui ensuite peuvent se propager très rapidement et provoquer une rupture brutale par fissuration. Ce phénomène, particulièrement dangereux, se produit par effets combinés de 3 paramètres :
- La température : la corrosion sous contrainte se développant rarement en dessous de 50°C.
- Les contraintes appliquées ou résiduelles subies localement par la pièce.
- La corrosivité du milieu : présence de Cl-, H2S ou milieux caustiques NaOH.
Les aciers austénitiques A4, sont plus résistants à la piqûre de corrosion que les aciers ferritiques au chrome.
En chevillage, la seule solution contre la corrosion sous contrainte reste l’acier HCR.